
Tato témata z úrazové chirurgie jsem sepsal jako podklad pro přípravu na státnici z chirurgie. Jsou zpracována dle znění aktuálních státnicových otázek.
Materiál také může sloužit jako neoficiální literatura k přípravě na atestaci z chirurgie.
Text nad rámec znalostí ke státní zkoušce (dle mého názoru) je uveden kurzívou. Slouží k lepšímu pochopení uvedených faktů nebo nabízí více informací pro zájemce.
Práce vznikla na nekomerční bázi pro vzdělávací a akademické účely. Tedy bez nároku na finanční odměnu.
Vypracoval: MUDr. Aleš Paclík
Obrázková dokumentace je použita s laskavým svolením AO Foundation.
Kresba: Ostatní obrázky jsou dílem MUDr. Evy Šimůnkové a MUDr. Aleše Paclíka
Editor: MUDr. Kristian Chrz
Bylo by fajn připomenout si, jak se vlastně zlomená kost hojí. Zároveň si uvědomíme, že poranění kosti je do určité míry spojeno s poraněním měkkých tkání. Mluvíme o přirozeném, tzv. sekundárním hojení kostí, s relativní stabilitou (konzervativní léčba, operační léčba s relativní stabilitou, žádná léčba).
Krevní zásobení kosti je zajištěno jednak periostálním řečištěm, které je napájeno drobnými cévami cestou úponu šlach a kloubního pouzdra, a druhak endostálním řečištěm – a. nutritiva proniká kostí do dřeňové dutiny a rozbíhá se jako cévní síť po endostu. Chirurg by se měl snažit maximálně tuto výživu respektovat (volit zavřené repoziční techniky, miniinvazivní přístup, nitrodřeňovou nebo přemosťující syntézu…pokud není nutná absolutní stabilita – viz kapitola o operační léčbě).
- v době úrazu dochází okamžitě ke krvácení z okrajů kosti, dřeňové dutiny, okolních měkkých tkání
- formuje se sraženina mezi úlomky a v okolí
- záhy dochází k vaskularizaci hematomu z okolních tkání a během cca 5 dnů je hematom nahrazen fibrovaskulární tkání = zánětlivá fáze.
- V reparativní fází se periostální buňky transformují na chondroblasty tvořící chrupavčitou tkáň. To vše za současného odbourávání drobných fragmentů pomocí osteoklastů. Osteoblasty zase produkují kolagen a během tří týdnů tu máme měkký svalek.
- Posléze se formují kolagenní vlákna a měkký svalek, opět za přispění osteoblastů, kalcifikuje – tvrdý kostěný svalek.
- svalek vzniká největší měrou právě díky aktivitě buněk periostu. Pokud je však krevní zásobení nedostatečné nebo dochází k nadměrnému pohybu na lomné linii, vzniká namísto kostěného svalku chrupavka. Periost je v tvorbě svalku aktivní jen několik týdnů.
- oblast dřeňové dutiny (endost) má též potenciál k vytvoření svalku. Endostální svalek je méně mohutný, ovšem jeho tvorba není časově omezena a trvá, dokud není kost zhojena.
Doba tvorby kostěného svalku závisí na faktorech jako je kvalita kosti, charakter zlomeniny nebo kvalita cévního zásobení.
Obecně lze říci, že spongiózní kost se hojí rychleji, svalek je vytvořen cca po 6 týdnech. Z toho plynou tyto příklady: částečnou zátěž při zlomené patě povolujeme za 6 týdnů, stejně tak v případě fraktury tibiálního plateau. Imobilizaci pro frakturu dist. radia snímáme za 5-6 týdnů. Klínovitá zlomenina obratlového těla toleruje axiální zátěž za 6 týdnů.
V případě kortikální kosti endostální svalek zraje i řadu měsíců a některé dlouhé kosti se hojí í 18 měsíců. Objemný periostální svalek však umožní časný návrat funkce. Např. diafýza humeru je pevně zhojena za cca 10 týdnů, diafýza tibie cca 16 týdnů. Naopak metakarpy, falangy a metatarsy jsou pevné za 4, 3 a 5 týdnů resp.
Název otázky začíná “komplikace zlomenin” – docela široké téma. Pojal bych to tímto rozdělením:
- Komplikace z delší imobility pacienta: hypostatická pneumonie, dekubity, hluboká žilní trombóza a plicní embolie, atrofie svalstva, dekalcinace skeletu a tvorba močových vápenatých konkrementů, močová infekce, depresivní ladění.
- Komplikace anestezie a operace: atelektáza a pneumonie, krvácení, iatrogenní poranění nervu, infekce operační rány, selhání vnitřní fixace
- Komplikace vázané přímo na zlomeniny: porucha hojení kosti, kloubní ztuhlost, avaskulární nekróza, Sudeckův syndrom, infekce kosti, poranění nervově-cévního svazku, pozdní ruptura šlachy.
Rozebereme si pár situací z poslední skupiny.
5.1 Poruchy hojení kosti
5.1.a. Opožděné hojení
Nejsou známky hojení kosti v době, kdybychom již hojení očekávaly. Dle lokalizace mluvíme o horizontu 3 – 6 měsíců. V případě konzervativního postupu či relativně stabilní OS není na RTG patrný svalek, na lomné linii je kost resorbována, ale okraje nejsou sklerotické. V případě absolutně stabilní OS je sledování obtížné, může se projevit uvolněním či prasknutím implantátu.
Projevuje se bolestí při zátěži a při pohybu v sousedních kloubech.
Léčba se odvíjí od několika scénářů:
- imobilizace byla neadekvátní -> upravíme imobilizaci a vyčkáme dalších 4-6 týdnů (riskujeme však zbytečně dlouhou nehybnost kloubů)
- imobilizace se zdá vpořádku -> konvertujeme na operační řešení
- opožděné hojení operované zlomeniny – > reoperace. Princip stejný jako u léčby pakloubů – zvýšit stabilitu a podpořit hojení.
5.1. b. Pakloub
Je to způsob hojení kosti, ale nešťastný. O pakloubu mluvíme, jestliže nedojde ke zhojení ani po dvojnásobku očekávané doby hojení (6 – 9 měsíců). Bez intervence je to ireverzibilní záležitost. Mezi fragmenty zůstává štěrbina vyplněna chrupavčitě-vazivovu tkání.
Základním klinickým projevem může a nemusí být bolest, stejně tak patologická hybnost a omezená hybnost v okolních kloubech
Klasifikací je několik, já bych se spokojil s rozdělením do tří klinicky významných skupin (zjednodušená klasifikace Chi Chuanova a Wen Jerova).
Zde si opět připomeneme, že předpokladem pro zhojení kosti je
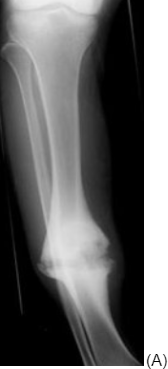
A) Hypertrofický pakloub. Kost měla dost výživy, ale neměla dostatečný klid na zhojení (nestabilní osteosyntéza, špatně zvolený konzervativní postup). Na RTG je patrná štěrbina, okraje fragmentů jsou sklerotické a mají zde větší průměr než sousední část kosti – svalek je excesivní a dobře prokrvený (obr. A). Problémem tedy není výživa, ale nedostatečná stabilita
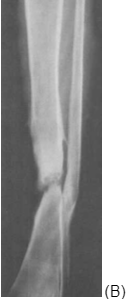
B) Atrofický pakloub. Oblast zlomeniny měla chudé cévní zásobení (otevřené zlomeniny, ztrátová poranění měkkých tkání, rozsáhlý otevřený operační přístup). Problémem je nedostatečná stabilita i výživa. Okraje fragmentů jsou úzké, zaoblené a porotické (obr. B). Atrofickým pakloubem se může projevit též infekce v oblasti zlomeniny. Dalším rizikovým faktorem je kouření.
Léčba. Nejčastějším způsobem řešení pakloubu je operace. U pacientů, kteří nejsou k operaci fit, je někdy využívána stimulace tvorby kosti elektrickými impulzy pomocí perkutánních elektrod. Procedura je několikaměsíční. Určitého efektu snad může dosáhnout i léčba ultrazvukem.
Pokud ale pacient nemá bolesti, funkce končetiny je pro něj dostatečná a zároveň pakloub dle anatomické lokalizace nepovede k předčasné artróze, tak nemusíme dělat nic.
U hypertrofickým pakloubů je principem operace zajistit dostatečnou stabilitu. Jí dosáhneme předvrtáním dřeňové dutiny, vpravením širokého hřebu a jeho zajištění šrouby s kompresí. Další možností je komprese fragmentů pomocí dlahy. Stabilita a komprese vedou k mineralizaci chrupavčitě-vazivové tkáně pakloubu za podmínky dobré vaskularizace.
V případě atrofických pakloubů musíme kromě stability zajistit i dobrou výživu a indukci tvorby kosti. Kromě rigidní osteosyntézy je třeba otevřenou cestou resekovat chrupavčitě-vazivovu tkáň a toto místo obložit štěpy spongiózy odebranými z jiného místa či štěpy získanými při předvrtávání dutiny. Tato spongióza indukuje místní tvorbu kosti pomocí svých mezenchymových buněk a osteoblastů a též slouží jako lešení pro novotvořenou kost. Lepšího efektu osteogeneze dosáhneme tzv. Judetovou dekortikací: dlátkem jsou v okolí původního pakloubu odsekány drobné povrchové plátky kortiky, které ovšem zůstávají v kontaktu s přilehlými měkkými tkáněmi.
C) Infikovaný pakloub. Infekce v místě zlomeniny inhibuje osteogenezi, pakloub je tedy zároveň atrofický. Infekce bývá komplikací otevřených zlomenin nebo vnitřních osteosyntéz (zde zánět vede k uvolnění osteosyntetického materiálu, tedy k nestabilitě a tedy k tvorbě pakloubu).
Klinicky může být okolí pakloubu zarudlé, oteklé a bolestivé. Velmi často je přítomen defekt měkkých tkání nebo secernující sinus.
Léčba spočívá v odstranění infikované tkáně radikální resekcí kosti a debridment okolí + antibiotika. Pro syntézu volíme zevní fixátor. Kostní defekt nad 3 cm po vymýcení infektu je možné řešit v současné době technikou dle Masqueleta: po stabilizací zevním fixátorem je kostní defekt vyplněn cementem. Po 10-14 týdnech je kolem něj vytvořena pseudosynoviální membrána a cement je vyměněn za spongiózní štěpy s následnou suturou membrány. Dalšími metodami řešení kostního defektu je tzv. kalusdistrakce na zevním fixátoru nebo kostní transfer na cévní stopce (část fibuly). Defekty měkkých tkání jsou vyplňovány muskulokutánními laloky po zvládnutí infekce. Definitivním krokem však může být amputace. Život s kvalitně oprotézovaným amputačním pahýlem může být mnohem snazší než s afunkční, bolestivou a páchnoucí končetinou.
Pseudoartróza je nezhojená zlomenina s nepravým kloubním pouzdrem produkujícím tekutinu a s okraji fragmentů pokrytými vazivově-chrupavčitou tkání. Léčba spočívá v resekci pseudopouzdra a vazivové tkáně, okrvanění a opracování konců fragmentů, spongioplastice a kompresi fixací zevní nebo vnitřní.
Klasickou klasifikací pakloubů je ta Weberova – Čechova:
- pakloub vitální (biologicky aktivní)
- hypertrofický: nedostatečná stabilita, nadměrný svalek (budí dojem koňského kopyta) nebo ještě více nadměrný (sloní noha)
- oligotrofický: malý kontakt fragmentů, svalek málo patrný
- pakloub avitální (bez biologické aktivity)
- atrofický
- defektní, nekrotický
- infikovaný

A – hypertrofický pakloub typu sloní nohy; B – hypertrofický pakloub typu koňského kopyta; C – oligotrofický pakloub; D – atrofický pakloub. Převzato z Wendsche P, Veselý R et al. Úskalí a komplikace při léčení zlomenin. Galén 2018.
5.1.c. Malpozice
Kost se hojí nebo se zahojila v postavení, které omezuje funkci a nebo je/bude pro pacienta diskomfortní.
Pokud angulaci, rotaci nebo zkrácení zachytíme velmi časně, můžeme situaci vyřešit opětovnou zavřenou repozicí a naložením adekvátní imobilizace. V době po zhojení fraktury je řešením korekční osteotomie, pokud není uspokojivé funkce dosaženo rehabilitací.
Zhojení ve zkrácení (dané též angulací) v případě horní končetiny málokdy činí obtíže. Humerus dobře toleruje i rotační odchylky. Radius či ulna zhojená ve zkratu však může významně omezit funkci prox. nebo dist. radioulnárního kloubu.
Zkrácení femuru (vč. zhojení fraktury krčku ve varózním postavení) nebo tibie do 1 cm je tolerováno dobře. Větší zkrácení se dá řešit zvýšeným podpatkem. Pokud je zkrácení způsobeno výraznou angulací, je vhodné stav řešit osteotomií k opětovnému nastolení symetrické zátěže na okolní klouby. Je dobré si uvědomit, že u seniorů zkrácení > 2cm zvyšuje při chůzi nároky na kyslík. Stoupá dechová i tepová frekvence, což pocítí zejména kardiaci.
5.2. Ztuhlost kloubu
Velmi častá komplikace zlomenin a jejich léčby. Dá se však minimalizovat. Příčiny se nachází uvnitř kloubu, poblíž kloubu nebo daleko od kloubu.
4.2.1. Intraartikulární příčiny:
- nitrokloubní adheze jako výsledek fibrotizace hemarthros v případě nitrokloubní fraktury
- mechanická blokáda kostním fragmentem
- poúrazová artróza; důvody: nerovnost kloubní plochy, avaskulární nekróza, malpozice zlomeniny vedoucí k nerovnoměrné zátěži kloubu
4.2.2. Periartikulární příčiny:
- postižení kloubního pouzdra či svalové manžety: fibróza z přímého poranění, otok,
- myositis ossificans (osifikace hematomu přítomného ve svalu v blízkosti zlomeniny; typicky u zlomenin oblasti lokte či po artroplastice kyčle)
- a samozřejmě: imobilizace kloubu při léčbě zlomeniny
4.2.3. Příčiny vzdálené od kloubu:
- tvorba adhezí mezi svalem a zlomeninou (např. m. kvadriceps a fraktura diafýzy femuru)
- svalová ischémie následovaná fibrózou a kontrakturou (Volkmann)
Prevence: adekvátní repozice fraktury; imobilizace jen těch kloubů, které je potřeba znehybnit a na nezbytně nutnou dobu; cvičení neimobilizovaných kloubů brzy po úrazu; elevace končetiny a restrikce otoku; brzká fyzioterapie tam, kde ztuhlost očekáváme.
5.3. Avaskulární nekróza (AVN)
Odumření části kosti z důvodu přerušení cévního zásobení. Čím větší dislokace, tím větší poranění přívodných cév a tím větší riziko AVN. Větší odumřelé fragmenty mohou hojení velmi zkomplikovat. Nejčastěji vídáme AVN hlavice femuru u intrakapsulárních zlomenin krčku, zlomenin anatomického krčku humeru nebo u dislokovaných zlomenin talu. Postižená nekrotická kost je měkká a mění tvar. To vede k bolestem, případnému ztuhnutí a sekundární artróze přilehlého kloubu. AVN se vyvíjí mnoho měsíců, v případě hlavice femuru i několik let. Klinické obtíže většinou předcházejí RTG obraz (sytější stín postižené kosti). K časnější diagnóze pomůže MRI.
Léčba: v případě významných klinických projevů. Pokud ke kompletní AVN ještě nedošlo, je možné aktivovat proces revaskularizace navrtáním postiženého okrsku. Další možností je nekrektomie a vložení spongiózního štěpu. V případě AVN části hlavice femuru je volbou korekce intertrochanterickou osteotomií. Při rozvinuté artróze je čas na artroplastiku.
5.4. Sudeckův algodystrofický syndrom
Ve světě se ujalo označení komplexní regionální bolestivý syndrom (CRPS). Jedná se o poruchu v oblast distální části končetin charakterizovanou bolestí, otokem, změnou teploty a barvy, omezenou hybností a kostní demineralizací. Spouštěcím mechanismem bývá zlomenina, poranění vazů či operace nejčastěji v oblasti zápěstí nebo hlezna. Projeví se cca 4 – 6 týdnů od insultu. Vzhledem k problematické diagnostice je incidence nejednoznačná, v USA je odhadována na 6/100 000 obyvatel/rok.
Patogeneze není zcela objasněna, pravděpodobně jde o dysbalanci vegetativního nervsta. Bolestí aktivovaný sympatikus vede ke konstrikci arteriol s následnou paralýzou kapilár. Výsledkem je lokální hyperémie, hypoxie, acidóza, zvýšená propustnost kapilár a další edém.
Postiženy jsou 2x častěji ženy, a ještě více ty postmenopauzální. Vyšší incidenci zaznamenáváme u jedinců psychicky labilních. Např. typickým kandidátem na Sudecka je žena s frakturou distálního radia chodící na kontroly opakovaně s flekčním držením poraněné paže, kterou si podpírá druhou rukou a neochotně si nechá na ruku při vyšetření sáhnout.
Dalším podpůrným faktorem mohou být
- příliš těsný sádrový obvaz
- opakované pokusy o zavřenou repozici
- nešetrné operování a operování v otoku
Diagnóza je založena zejména na klinice a jejím základním předpokladem je trvalá bolest nepřiměřeně velká původnímu inzultu. Dále musí být přítomny min. 3 z následujících 4 znaků/příznaků:
- hyperestézie a/nebo alodynie
- změna teploty (CRPS má teplou i studenou variantu) a/nebo změna barvy kůže (lividní, červená)
- otok a/nebo zvýšená potivost
- omezená hybnost nebo slabost/třes nebo trofické změny kůže/nehtů/ochlupení
- Kostní scintigrafie může prokázat vyšší metabolickou aktivitu periartikulárně při kloubech distálně od insultu, ale její negativní výsledek diagnózu CRPS nevylučuje.
- Na prostém RTG po několika týdnech je patrná kostní demineralizace.

Všimněte si flekčního držení prstů, otoku, atrofie kůže a hypertrichózy na levé ruce. Naopak lividní zbarvení kůže je patrné v případě levé nohy.
Vývoj:
- Stádium I: zánět – bolest trvající nepřiměřeně dlouho od úrazu, otok, proteplení, zarudnutí, resorpce kosti. Trvá i měsíce.
- Stádium II: atrofie svalů a kůže, otoky trvají, horší se hybnost, kůže chladne
- Stádium III: dystrofie po roce trvání potíží – kontraktury, ztuhnutí kloubů, cyanóza a chlad aker, bolest mizí
Léčba má lepší výsledky, pokud započne co nejdříve po diagnóze. Stádium I je ještě reverzibilní. Základní kameny jsou:
- fyzioterapie: množství metod LTV k obnovení rozsahu pohybu, zamezení kontraktur, antiedematozní opatření; doplněno o vodoléčbu
- současná farmakoterapie k redukci bolesti vedená v ambulanci pro léčbu bolesti: NSAID (ibuprofen) + tlumení neuropatické bolesti (gabapentin, někdy tricyklická antidepresiva).
Doplňkovou léčbou můž být secatoxin (sympatolytikum), vitamin D + kalcium, magnézium, případně bisfosfonáty při trvající bolesti v časných stádiích a pozitivní scintigrafii. Menší studie prokázaly benefit glukokortikoidů (p.o. prednison) v stádiu II. - psychosociální terapie při neefektivní léčbě po 2 měsících
- Hyperbarická komora (jde přece o hypoxii)
- Pokud výše uvedená léčba je neúčinná, nabízí se několik invazivních alternativ s nejistými výsledky: blokáda regionálního sympatického ganglia (lidocain do g. stellatum či lumbálních ganglií), neuromodulační spinální stimulace, chirurgická sympatektomie.
Prognóza: I. stádium je při včasném záchytu a léčbě reverzibilní. Avšak dle studií po 6 letech od diagnózy bylo cca 30% bez obtíží, 40% se vrátilo do své původní práce.
5.5. Volkmannova ischemická kontraktura
Jedná se o následek nerozpoznaného či špatně léčeného kompartmentového syndromu předloktí, kdy dochází k prolongované ischémii volární skupiny svalů předloktí, fibrotizaci a konečně kontraktuře. Ischémie je dána zvýšeným tlakem v osteofasciálních prostorech v oblasti lokte z důvodu otoku a hematomu. Někdy je popisována jako iatrogenní poškození z důvodu příliš těsného naložení sádrového obvazu. Byť je tato komplikace naštěstí vzácná, její následky jsou tragické a trvalé. Mají typický obraz: flekční kontraktura lokte, předloktí v pronaci, zápěstí a prsty v palmární flexi s nemožností pasivní extenze, metakarpofalangeální klouby v extenzi.

Volkmann popsal tento stav jako komplikaci dislokovaných extenčních suprakondylických fraktur humeru u dětí. Je ovšem třeba bedlivě sledovat prokrvení periferie u zlomenin humeru a diafýz předloktí v každém věku.
Prevence spočívá v řádné, ale šetrné repozici dislokované zlomeniny a dostatečné stabilizaci. Při rozvinutém kompartmentovém syndromu neváháme provést včasnou fasciotomii postižené svalové lóže.
Léčba je obtížná, málo úspěšná a zahrnuje excizi fibrotické tkáně, tenolýzu, neurolýzu, kapsulotomii, přenosy nervových štěpů, případně svalových laloků.
VYPRACOVÁVANÁ TÉMATA Z TRAUMATOLOGIE:
- 01. Úraz. Mechanismy vzniku, charakteristika a prevence (ver. 2024)
- 03. Operační léčba zlomenin, indikace k operaci, druhy osteosyntéz a náhrad. (ver. 2024)
- 04. Konzervativní (neoperační) léčba zlomenin. (ver. 2024)
- 05. Komplikace zlomenin, poruchy hojení, infekce, Sudeckův syndrom a Volkmannova ischemická kontraktura (ver. 2024)
- 06. Kompartmentový syndrom (ver. 2024)
- 08. Bodná a střelná poranění (ver. 2024)
- 09. Principy léčení otevřených zlomenin, klasifikace (ver. 2024)
- 12. Poranění kloubů, vymknutí kloubů (ver. 2024)
- 14. Poranění pánve (ver. 2024)
- 16. Orofaciální poranění (ver. 2024)
- 17. Poranění hrudníku (ver. 2024)
- 18. Úrazové hemoperitoneum (ver. 2024)
- 19. Poranění sleziny a jater (ver. 2024)
- 20. Zlomeniny lopatky (ver. 2024)
- 23. Zlomeniny horního konce pažní kosti (ver. 2024)
- 24. Zlomeniny diafýzy pažní kosti (ver. 2024)
- 25. Zlomeniny distálního konce pažní kosti (ver. 2024)
- 27. Zlomeniny okovce loketní kosti (ver. 2024)
- 29. Diafyzární zlomeniny předloktí (ver. 2024)
- 31. Zlomeniny a luxace karpálních kostí (ver. 2024)
- 32. Zlomeniny kostí záprstních a článků prstů (ver. 2024)
- 33. Klasifikace a léčba zlomenin horního konce stehenní kosti (ver. 2023)
- 34. Zlomeniny diafýzy stehenní kosti (ver. 2024)
- 35. Zlomeniny dolního konce stehenní kosti (ver. 2024)
- 38. Zlomenina horního konce holenní kosti (ver. 2024)
- 39. Zlomeniny diafýzy holenní kosti (ver. 2024)
- 41. Zlomeniny kotníků a poranění vazů hlezenního kloubu (ver. 2024)
- 44. Popáleniny (ver. 2024)
- 45. Hromadné neštěstí, zásady etapového dělení, systém START (ver. 2024)
- 46. Soudobá válečná poranění (ver. 2024)



Buďte první kdo přidá komentář